【产品名称】
通用名:非结核分枝杆菌核酸检测试剂盒(荧光 PCR 法)
【包装规格】
货号:PR35351
规格:25 人份/盒,50 人份/盒。
【预期用途】
本试剂盒用于非结核分枝杆菌(NTM)核酸的定性检测,用
于非结核分枝杆菌感染的辅助诊断及流行病学监控。
【检测原理】
本试剂盒根据荧光 PCR 技术原理,针对非结核分枝杆菌设
计特异性引物和 Taqman 探针,通过荧光 PCR 检测仪进行检测,
从而实现对非结核分枝杆菌的检测。
【主要组成成分】
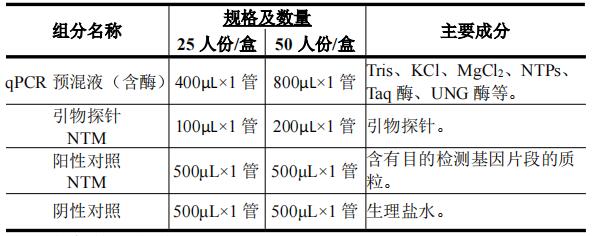
【储存条件及有效期】
1.避光-20℃±5℃储存,有效期 12 个月。
2.采用泡沫箱加冰袋的运输方式,运输不超过 4 天;开封后避
光-20±5℃储存;反复冻融不超过 6 次。
3.生产日期、有效期至:见外包装盒。
【适用仪器】
适用于 ABI 7500、Bio-Rad CFX96、Roche Lightcycler480I、
Lightcycler480II、cobas Z480、宏石 SLAN-96S、SLAN-96P
等实时荧光定量 PCR 仪。
【样本要求】
1.样本种类:鼻/咽拭子、痰液、支气管肺泡灌洗液;组织培养
物等样品。
2.保存条件:采集的标本应及时送检,24 小时内检测的应 4℃
保存,超过 24 小时的最好-70℃保存(如无-70℃保存条件,
待测样本可于-20℃冰箱保存 10 天),并避免反复冻融。
【检测方法】
1.试剂准备(试剂准备区)
将试剂盒各组分室温融化,充分振荡混匀后瞬时离心。计算
试剂使用份数 N(N=样本数+1<阳性对照>+1<阴性对照>),根据
下表配置反应体系,将各组分加入至同一适当体积离心管中,充
分混匀后瞬时离心,配制成反应体系混合液,按 20μL/孔分装至
PCR 反应管/板,并转移至样本处理区。

2.样本处理(样本处理区)
① 核酸提取
选择合适的核酸提取试剂盒提取样本核酸,具体按照相应的
试剂盒说明书操作。
② 加样
在已加入反应体系混合液的 PCR 反应管/板上分别加入处理
好的待检标本核酸、阴性对照、阳性对照各 5μL,终体积为 25μL。
盖紧管盖或封膜,瞬时离心后置荧光 PCR 扩增仪上检测。
3.扩增检测(核酸扩增区)

*步骤②中 55℃时荧光检测,检测通道为 FAM。
*ABI 系列荧光 PCR 仪不选 ROX 校正,淬灭基团选 None。
4.结果分析
根据分析后图像调节起止值,(建议起始设在 3~15、终止设
在 5~20,同时调整阴性对照的扩增曲线平直或低于阈值线),点
击分析,在报告界面查看结果。
【质量控制】
1.阴性对照:Ct 值>38 或未检出。
2.阳性对照:扩增曲线呈典型 S 型,且 Ct 值≤35。
3.同一实验以上要求需同时满足,否则本次实验视为无效。
4.每种检测靶标都需设阴阳对照,不同的靶标根据对应阴性调
整基线阈值。
【结果判读】
1.各通道检测靶标。

2.阴性:Ct 值>38 或未检出。
3.阳性:扩增曲线呈 S 型,且 Ct 值≤35。
4.疑似阳性:扩增曲线呈典型 S 型,且 35<Ct 值≤38,需复检;
复检结果若一致,判定结果为阳性,若 CT 值>38 或未检出,
判定结果为阴性。
【检验方法的局限性】
1.样品采集、运输、保存不当,试剂运输、保存、配置不当都
可能会影响实验结果,甚至会导致假阴性结果。
2.如果实验室污染、试剂污染、样品交叉污染,可能出现假阳
性结果。
【试剂盒性能指标】
1.最低检测限:500 copies/mL。
2.特异性:针对可能与检测靶标产生交叉的其他病原无交叉反
应。
【注意事项】
1.PCR 操作各阶段应严格分区操作,避免交叉污染。
2.试剂盒各组分使用前应充分融化混匀,离心数秒后使用。
3.各组分不得与其他产品或不同批号的相应成分进行互换。
4.待测标本若不及时检测,应保存于-70℃。
5.样品的处理应该严格按照生物安全规范操作。
6.PCR 操作人员应具有经验和受过专业培训。
7.本试剂盒仅用于科研使用,不做为临床诊断使用。